多系统萎缩
Neuropathophysiology[|]
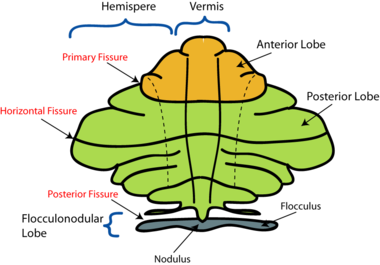
神经病理学上,MSA的特征是硬核、桥脑和小脑萎缩。
神经病理模式的复杂性与临床表型谱相关(MSA-P和MSA-C之间可以观察到一些重叠,每个亚型都有特定的神经病理特征)
子类型
MSA-P和MSA-C都以神经系统的其他区域受累为特征,包括脊髓中间外侧柱、迷走神经背核和Onuf核[3].运动皮质和辅助运动皮质也有牵连。
病因[|]
MSA的原因尚不清楚;然而,对于其他神经退行性疾病,基因和环境机制的复杂相互作用似乎是可能的。[4]
假设包括[3](从2019年评审)
- α突触核蛋白在少突胶质细胞中的积累,包括SNCA表达、神经元少突胶质细胞蛋白转移、蛋白降解受损和α -突触核蛋白扩散机制。
- [5]
- GCI被认为类似于运动障碍中出现的神经纤维缠结。
- 神经缠结是在神经元中发现的病理蛋白群,它会缓慢地对中枢神经系统中的神经元造成损伤。
胶质细胞增生也是MSA的一个原因:
- 一旦中枢神经系统受到损伤(由GCI的形成造成),神经胶质细胞就会介入修复损伤。[5]图示胶质细胞增生
- 然后形成神经胶质疤痕,以保护和开始愈合受损的中枢神经系统。它能有效抑制进一步的损伤,但也会阻止神经再生。疤痕细胞分泌了许多神经发育抑制分子,阻止了中枢神经系统的完全物理和功能恢复。[5]
- 这就形成了一个损伤(来自GCI)和无效愈合(通过胶质细胞分裂)的重复循环,这将导致ANS和CNS的控制越来越差。[6]
虽然上述过程是目前许多研究者的一种想法,但细胞最初丢失过程的病因尚不清楚。[5]
流行病学[|]
MSA是一种孤儿病[4]
- 建立:年龄估计在1.9至4.9之间,40岁以后可能高达7.8。Wenning等人完成了对100例MSA患者的分析,并测量了他们的残疾。结果显示,MSA患者的致残速度比帕金森患者快。[7]
- 发病率:
- 每10万人年0.6-0.7例,范围为每10万人年0.1 - 3.0例。来自俄罗斯和瑞典北部的研究报告,发病率分别为0.1和2.4 / 10万人年。
- 年龄在70岁以上的人中,每10万人中有12人会增加。
- 在西半球,MSA-P约占70 - 80%
- MSA-C在亚洲人群中更为常见,约占67-84%。
- 运动症状的发病时间为56±9年,男女均受影响。然而,与帕金森病一样,20 - 75%的MSA病例具有前驱/临床前阶段,伴有非运动症状,包括心血管自主功能衰竭、泌尿生殖和性功能障碍、体位性低血压、快速眼动睡眠行为障碍和呼吸障碍,这些症状可能先于运动症状数月至数年
- MSA多见于男性而非女性(Diedrich)。[5]
特征/临床表现[|]
MSA根据患者表现出的最主要症状进行分类。
MSA-A:
图3:自主神经系统
MSA-P:
MSA-C:
- 当小脑功能障碍更加突出时,该疾病被标记为MSA-C。超过50%的MSA患者会出现小脑功能障碍。[8]
- MSA的小脑特征最初表现在躯干和下肢,导致步态紊乱。[9].这些患者还表现为肢体动态性共济失调和扫描构音障碍,以及小脑性共济失调。
其他症状:
相关并发症/系统性的参与[|]
- 认知和心理健康水平[10]
- 通常没有明显的认知障碍。痴呆被认为在MSA中很罕见,但可能影响12%到18%的患者
- 情绪不稳定可能发生在疾病发展的后期。[8]
- 抑郁、焦虑、恐慌发作和自杀意念可能出现在MSA中。有些患者会表现出不恰当的笑或哭。高达75%的患者可能出现认知障碍,特别是在执行功能方面
- MSA患者很难将注意力从一种刺激转移到另一种刺激,[9]目标导向的认知能力下降。
2.排便和膀胱功能障碍:
3.随着疾病进展出现的症状:
4.吞咽困难和构音障碍是该病晚期的症状[9]应该接受语言障碍治疗。
诊断测试/实验室测试/实验室值[|]
目前,还没有具体的症状、血液测试或影像学研究来区分MSA。相反,医生依靠症状史、体格检查和实验室测试的结合来评估运动系统、协调和自主功能,从而得出可能的诊断[10].
- 功能性磁共振成像(fMRI)等医学技术可以测量大脑的活动水平,并可以显示大脑功能受损的区域。见下图MRI图像。
- 通过将敏感的模式识别技术应用于某些MRI研究,医学科学越来越多地将MSA的早期症状与帕金森病和其他神经系统疾病进行更精确的区分。
- 新的研究还发现,在MSA患者中,一种对髓磷脂的产生很重要的特殊类型的脂质运输分子可能存在缺陷,对这种被称为ABCA8的分子进行评估,可以为MSA提供病因解释和筛查工具。
图4: MRI显示桥脑(A)和小脑(B)区明显萎缩。
诊断挑战[|]
将MSA与PAF(纯自主性衰竭)和纯帕金森症区分开来是很重要的。由于这种疾病没有“典型”的表现,MSA通常可以被其他诊断所掩盖,因此,如果有纯帕金森、PAF等患者,就必须密切注意与该诊断无关的任何可疑S/S。这是中肯的,这样这些病人就不会被误诊。
- MSA患者最常被误诊[1]
- 只有25%的MSA患者在第一次神经系统检查时得到正确诊断。正确的诊断通常在发病后的平均4至5年确立。[7]
- MSA和帕金森症之间的区别是通过排斥来实现的。如果没有自主神经或小脑体征,那么患者极有可能是单纯的帕金森症。[1]
- 90%的MSA-P患者[7]这是一个迹象,该患者不是单纯的帕金森症,因为左旋多巴是无效的。
- 体位性低血压、排尿困难、快速进展的功能限制、呼吸大声和阳痿表明MSA是比帕金森病更可能的Dx。[7]
- 如果患者存在ANS S/S(如体位性低血压),但没有帕金森症或共济失调的迹象,则最有可能患有PAF。[1]
医疗管理[|]
MSA必须根据临床表现的概率进行诊断。[6]
迄今为止,没有任何致病或改善疾病的治疗方法,对症疗法也很有限。迫切需要阐明MSA的致病机制,以便制定新的治疗策略[4].
- 据报道,83%的MSA-P患者最初有左旋多巴反应,但效果通常是短暂的,只有31%的患者表现出持续3.5年的反应。在一些患者中,可观察到运动波动伴随磨损现象或脱界肌张力障碍。
- MSA不推荐深部脑刺激
- 主动免疫αS和联合抗炎治疗可能是一种很有前途的治疗策略。基于MSA联盟已完成或正在进行的干预试验,针对αS的新策略正在进行中。
临床表现不仅对MSA的诊断很重要,而且对治疗也很有帮助。由于MSA是一种可变的疾病,最有效的医疗管理是对症治疗。[6]目前的医疗管理包括药物治疗。药物是根据MSA的亚型和出现的症状而开的。
因为MSA是一种可变的疾病,可以表现为许多不同的方式。因此,治疗是对症治疗。
药物治疗:MSA-A
为了控制自主症状,患者可以考虑增加盐的摄入量或服用类固醇激素或其他提高血压的药物。[10]
- 治疗[6]可以开一些药物来加强血管收缩,增加血容量,从而使血压升高(氟氢可的松而且米多君).[1]
- 对于治疗便秘的大便软化剂药物是有效的。[6]
- 为了治疗尿功能障碍,药物干预不能充分减少MSA患者的尿空后残留体积,但抗胆碱能药物如Oxybutynin可以改善反射过度的症状[7]
- 治疗阳痿:西地那非(25 ~ 75mg)可成功治疗勃起功能障碍。[7]
MSA-C
- 目前还没有建立小脑性共济失调和锥体功能障碍的药物治疗策略。[7]
MSA-P
- 用于治疗帕金森病的药物可以缓解某些MSA患者的肌肉僵硬、行动迟缓和其他运动症状,但仅限于早期阶段,效果不如帕金森患者。帕金森病药物也能降低血压,并可能加重NOH症状、头晕和昏厥发作。[10]
物理治疗管理[|]
物理疗法提供了不含药物的工具来保持肌肉强壮和灵活,帮助预防[10].
治疗性运动/活动:
- 根据Wedge等人的一项研究,[8]
- 抵抗训练已被证明对MSA患者有效。
•膝关节伸肌和屈肌、髋关节外展肌和内收肌、踝关节植物屈肌是阻力训练的目标。选择这些肌肉群是因为它们对平衡的重要性。[8]
•在抗阻训练干预后,患者的步态模式明显改善(即使在疲劳时也能保持良好的步高和步长)。减少宴会步态和其他功能的改变。患者改善了转移技术和姿势(即良好的头部和躯干在坐姿和站姿)。也减少了[8]
额外的物理治疗建议:
研究强化了这一事实,因为MSA是一种可变障碍。每个MSA患者表现不同,因此很难给出明确的PT建议。
- 根据患者的活动能力和功能水平,PT应该运用他们的技能和知识为患者创造一个安全和最佳的环境。
- 作为一名PT,尽可能长时间地保持力量和生理健康对患者来说是最有价值的。[1]
- 对患者和家属进行关于PT益处的教育对患者/家属的知识和依从性很重要。
- 让PT目标更现实。将目标建立在当前功能的基础上,并考虑到对患者最重要的活动。
- 由于这是一种进行性障碍,PT患者必须经常重新评估目标,以确保它们是适当的。
鉴别诊断[|]
MSA常表现为以下疾病:
预后和前景[|]
目前的预后是保守的,大多数MSA患者在症状出现后的6-10年内离开了疾病或其并发症。尽管如此,仍有理由对MSA的研究抱有希望。由于MSA的生物学可能与其他神经退行性疾病(如帕金森病)有关,针对其他情况设计的治疗方法也可能对MSA患者有帮助。[10]
案例报告[|]
阻力训练对多系统萎缩患者平衡和功能能力的影响。老年物理治疗杂志2008;31:79-83。
以下病例报告记录了一个有2年MSA病史的68岁女性患者的阻力训练计划的影响。
hy- drager综合征:多系统萎缩伴抑郁。心身医学。2005;46:73-6。
下面的病例报告讨论了在诊断过程中的一些斗争的48岁男性MSA。
masidori T, Yamanishi T, Yoshida K, Sakakibara R,Sakurai K, Hirata K.持续尿失禁是多系统萎缩的收缩逼尿肌和内在括约肌缺陷的初始症状。国际泌尿学杂志。2007;14:972-74。
以下病例报告说明尿失禁如何成为MSA的第一个症状的66岁女性。
后藤K, Ueki A, Shimode H, Shinjo H, Miwa C, Morita, Y.多系统萎缩中的抑郁:一个病例报告。精神病学与临床神经科学。2000;54:50 07-11。以下病例报告说明抑郁症如何成为一名56岁女性MSA的最初症状。
资源[|]
SDS / MSA支持组
参考文献[|]
- ↑1.01.11.21.31.41.51.6神经科学:康复基础。第三版。圣路易斯:桑德斯·爱思唯尔,2002。
- ↑MSA联盟。MSA可从何处获得:https://www.youtube.com/watch?v=mVqiCgaLSf4&app=desktop(最后访问17.1.2020)
- ↑3.03.1Compagnoni总经理,Di Fonzo A。了解多系统萎缩的发病机制:现状和未来展望。Acta neuropathologica通信。2019年12月,7(1):113。可以从:https://actaneurocomms.biomedcentral.com/articles/10.1186/s40478-019-0730-6(最后访问16.1.2020)
- ↑4.04.14.2冻结卡。多系统萎缩:一种少突胶质神经共核病.中华医学会老年痴呆症杂志,2018年1月1日;62(3):1141-79。https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5870010/(最后访问16.1.2020)
- ↑5.05.15.25.35.45.55.6多系统萎缩症。范德比尔特大学医学院2009。http://emedicine.medscape.com/article/1154583-overview(2010年1月24日访问)。
- ↑6.06.16.26.36.46.56.6哈迪,乔安妮。多系统萎缩:病理生理学、治疗与护理。护理标准2008;22:50-6。
- ↑7.07.17.27.37.47.57.67.77.8多系统萎缩的病理生理学和治疗。中枢神经系统药物2001;15:839-48。
- ↑8.008.018.028.038.048.058.068.078.088.098.108.11阻力训练对多系统萎缩患者平衡和功能能力的影响。老年物理治疗杂志2008;31:79-83。
- ↑9.009.019.029.039.049.059.069.079.089.099.109.11王晓燕,王晓燕。多发性系统萎缩。物理治疗杂志1999;79:488-94。
- ↑10.010.110.210.310.410.5MSA联盟。MSA你需要知道的4.4.2019.可以从:https://www.multiplesystematrophy.org/wp-content/uploads/2019/09/What-You-Need-to-Know-9.4.19-DSC-AM-NV-Edits2.pdf(最后访问17.1.2020)
- ↑奥沙利文SS,梅西LA,威廉姆斯DR, Silveira-moriyama L,肯普斯特PA,霍尔顿JL, Revesz T,李斯,AJ。进展性核上麻痹和多系统萎缩的临床结果。大脑。2008;131:1362 - 72
- ↑海TC。多系统萎缩。2010。http://www.dizziness-and-balance.com/disorders/central/movement/msa.html(2010年4月5日访问)。